|
Gen Klonlaması (Moleküler Klonlama) Prof. Dr. Mustafa Arda
Ankara Üniversitesi
Veteriner Fakültesi 01. Genel
Bilgiler Rekombinant DNA
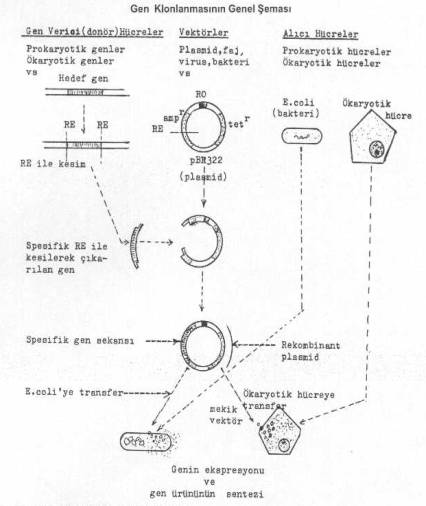
teknolojisinin başlıca uygulama yöntemleri arasında gen klonlamasının önemi ve yeri
çok fazladır. Hatta, esasını oluşturur. Gen klonlaması, basit olarak, bir genin
identik kopyalarının elde edilmesi veya bir bireyden orijin alan identik projeni
gruplarının oluşturulması olarak tanımlanabilir. Bir tek bakterinin uygun katı besi
yerinde üreyerek milyonlarca identik nesil oluşturması ve gözle görülebilecek koloni
meydana getirmesi de buna örnek verilebilir. Ancak bu tanım, bugün biyoteknolojide,
aşağıdaki tarzda uygulamaya konulmaktadır. Önemli bir ürünün (veya proteinin)
sentezini kodlayan genin ait olduğu hücre (prokaryotik veya ökaryotik) genomundan (veya
kromozomundan) özel yöntemlerle (genellikle, restriksiyon endonukleaz enzimleri ile)
kesilerek çıkarılması, bunun bir taşıyıcı (vektör) DNA'sı ile birleştirilerek
alıcı bir hücreye (prokaryotik veya ökaryotik) transfer edilmesi, bu alıcı hücrede
genin ekspresyonunun sağlanmasıdır.
Yukarıda kısaca tarif
edilen klonlamanın olumlu sonuç verebilmesi, konu üzerinde çalışanların bilgi,
becerisi ve kullanılan yöntemlere bağlıdır. Birçok aşamalardan oluşan teknoloji,
bu basamakların uyumlu işbirliği ile gerçekleştirilir. Gen klonlamasında
önemli olan aşamalar kısaca şöyledir (genel prensipler). 1) Gen taşıyan DNA'nın
(veya RNA) saf olarak elde edilmesi, 2) Genin yerinin belirlenmesi, 3) Genin çıkarılması, 4) Taşıyıcı (vektör)
DNA'nın elde edilmesi, 5) Gen DNA'sının vektör
DNA'sı ile birleştirilmesi, 6) Oluşan rekombinant vektör
DNA'nın alıcı hücreye aktarılması, 7) Seleksiyon, 8) Gen ürününün kontrol
edilmesi. 02. Gen taşıyan
DNA (veya
RNA')nın Elde
Edilmesi Klonlamanın ilk ve
önemli aşamasını oluşturan bu kısımda, istenilen ürünün iyi tarzda sentezini
kodlayan geni içeren prokaryotik (veya ökaryotik) hücre genomunun (DNA veya RNA) saf ve
bol olarak elde edilmesi yer almaktadır. Ayrıca, gen bankalarından da yararlanılabilir. İstenilen geni
taşıyan hücre bakteri
ise, bu mikroorganizma katı kültür ortamlarında üretilerek, tür özelliklerini tam
olarak gösteren tek bir koloni seçilir ve bunun sıvı ortamda saf kültürü yapılır.
Sonra, logaritmik üreme döneminde kültür santrifüje edilerek çöktürülür, tortu
birkaç kez yıkanır ve bir süspansiyon elde edilir. Bu süspansiyon özel yöntemlerle
(kaynatmak, alkali ile muamele, SDS, vs.) lize edilir. Ayrıca, lizozim, proteinaz, RNaz, SDS,
tris ve EDTA karışımı da kullanılarak, hücre
duvarı, sitoplasmik organeller, ribosom ve proteinlerin giderilmesi sağlanır. Sonra,
ekstrakt pürifiye (etanol, kloroform) edilerek saf DNA
süspansiyonu elde edilir. Aynı amaç için diğer yöntemlerden biri de seçilebilir. DNA diğer hücre
komponentlerinden daha kolay ve saf separe edilebilir. Çünkü: DNA'nın kendine özgü
bir kimyasal yapısı ve fiziksel özellikleri vardır. Şöyle ki: 1) Bakterilerde
kromozom uzunluğu oldukça büyüktür. Örn., E. coli 'de kromozom 1.1 - 1.4 mm uzunluktadır. Bakteri DNA'sında intron bulunmadığı için, genleri kullanmak daha
kolay olmasına karşın ökaryotik hücre DNA'sında intronların varlığı bunların
doğrudan kullanılmasına engel teşkil etmektedir. Bu dezavantajları gidermek için,
hücrelerdeki olgun mRNA'lardan yararlanılır. Çünkü, bunlarda intron bulunmamakta ve
sadece kodlayan eksonlardan
oluşmaktadır. Revers transkriptase enzimi yardımı ile cDNA'ya çevrilerek
kullanılırlar. Plasmid
DNA'sı
hazırlamak için de, sitoplasmasında plasmid içeren konak hücre (bakteri) uygun
koşullarda üretilerek, kolonilerden saf sıvı kültürler elde edilir. Bu sıvı
kültürleri, bakteri içinde plasmid replikasyonunu artırmak için, 300 mikrogram / ml spectinomycin veya 150 mikrogram / ml chloramphenicol ilave edilerek 16-20 saat etkide
bulundurulur. Sonra, yukarıda bakteride bildirilen işlemler aynen uygulanarak bakteriler
lize edilir ve bunlardan plasmid ve bakteri DNA'sı ekstre edilerek alınır. Sonra,
içinde Cesium chloride ve Ethidium bromide bulunan bir tüpe konarak
santrifüje edilir. Bu işlemin sonucunda kromozomal DNA üstte plasmid DNA altta
toplanır. Buradan plazmid DNA'sı toplanarak alınır. Eğer daha fazla plasmide ihtiyaç
varsa, tekrar bunlar, CaCI2 ile permeable hale getirilmiş E. coli 'ye transfer edilir ve fazlaca üretimi
sağlanır veya yeterli ise denemelerde kullanılır. Plasmid DNA'sı elde etmede ve
saflaştırmada başka yöntemlerden de yararlanılabilir. Bazı plasmidler de
(pUC serisi) çok çabuk ürediğinden büyük bir sorun ortaya çıkarmazlar. Viruslara ait genetik materyal
(DNA veya RNA) hazırlamak için bir çok basit veya komplike yöntemler bulunmaktadır.
Araştırıcılar kendilerinin olanak ve tecrübelerine göre en uygununu seçmek
durumundadırlar. Önemli olan nokta, virusların bol ve saf olarak elde edilmesidir. Bu
amaçla, virus süspansiyonlarına, etrafındaki protein tabiatındaki kapsidi veya,
zarflı viruslarda da zarfı gidermek için bazı kimyasal maddelerin ve solüsyonların
katılmasıdır. Genellikle, DNA ve RNA
viruslarında, viruslar santrifugasyonla klasifiye edildikten sonra, tüpteki
süspansiyona SDS, Proteinaz K, fenol, kloroform,
isopropanol, izoamil alkol, etanol, EDTA
gibi bazı kimyasal maddeler ilave edilerek viruslar etrafındaki protein tabakasından
kurtarılarak sadece DNA veya RNA'lar elde edilebilir. Bakteriyofajlar için de saptanmış
benzer yöntemlerden birinden yararlanılır. Genler her zaman
genomik DNA veya RNA da bulunmadığı göz önüne alınarak, gerekli durumlarda hücre
içindeki mRNA'dan
da aynı derecede yararlanılabilir. Ökaryotik
hücrelere
ait genlerin elde edilmesi de yine benzer fakat özel yöntemler kullanılarak DNA'ları
ekstre edilir ve saflaştırılır. Sonra, RE'lerden uygun olanlarından biri ile
kesilerek gen taşıyan segmentler elde edilir ve bunlar klonlamada kullanılırlar. Not: Bakteri, virus, plasmid,
faj vs. DNA'larını saf olarak elde edebilmek için bir çok prosedür hazırlanmış ve
pratiğe konulmuştur. Bunlardan birinin seçimi ve kullanılması araştırmalara
bağlıdır.
Her ne kadar genin
yerinin belirlenmesi mümkünse de, klonlamada genellikle, istenilen geni taşıyan
DNA'nın (veya kısa segmentlerinin) saf bir süspansiyonunun hazırlanması, amacı
gerçekleştirmede yeterli olabilmektedir. Genlerin elde
edilmesinde ve yerlerinin saptanmasında bazı yöntemlerden yararlanılır. Bunlar da
kısaca şöyledir: 1) İn vitro sentez: Eğer istenilen gen ürünü
bir protein ise ve yapısı (amino asit sayısı, türü ve sırası) biliniyorsa, bu
proteini kodlayan DNA sekanslarını belirleyerek in vitro koşullarda sentezini sağlamak
mümkündür. Bu tarzda elde edilen DNA segmenti, klonlamada başarı ile kullanılabilir.
Örn., insülin
ve somatostatin
hormonlarını kodlayan genlerin in vitro sentezleri gibi. Bu yöntem başarılı
olmasına karşın zaman alıcı ve masraflıdır. Çok miktarda amino asit sayısına
sahip olan proteinleri kodlayan DNA segmentleri, ayrı ayrı sentezlendikten sonra
birleştirilirler. Son yıllarda, özel aletler (DNA
sentetizerler) yardımı ile istenilen uzunlukta DNA sekansları kolayca sentez
edilebilmektedir. 2) Hibridizasyon yöntemleri: Bu teknikler daha
ziyade gen taşıyan DNA sekanslarının yerlerini belirlemede kullanılmaktadırlar. En
fazla yararlanılan yöntemler şunlardır: a) Southern blot hibridizasyonu: Bu teknikte,
materyallerden elde edilen ve bir RE ile kesimi yapıldıktan sonra oluşan saf DNA
segmentlerinin agarose jel elektroforezde seperasyonu yapılır. Agarose jelden sonra
nitroselüloz filtresine transfer edilerek burada, işaretli
(32P, biotin)
problar kullanarak hibridizasyon sağlanır
ve otoradiografik veya renk oluşumuna göre genin yeri belirlenir. Konu üzerinde ileriki
bahislerde ayrıntılı bilgi verilmektedir. Yeri saptanan DNA
segmenti, agarose jel üzerinden çıkarılarak klonlamada kullanılır. b) Northern blot hibridizasyon: Bu yöntemde,
agarose jel üzerine RNA separe edilerek işlemler aynen Southern blotta olduğu gibi
devam ettirilir. Hibrid molekülleri ortaya koymada da işaretli DNA veya RNA
problarından yararlanılır. 3) İstenilen genler
her zaman DNA üzerinde değildir. Genetik materyal olarak RNA taşıyan viruslarda,
genler RNA da bulunurlar. Böyle durumlarda tek iplikçik viral RNA saf olarak elde
edildikten sonra, buna revers transkriptaz (RT)
enzimi ile tek iplikcikli komplementer DNA (cDNA) sentezlenir. Bu RNA-DNA kompleksinden
RNA çıkarıldıktan sonra, bu cDNA iplikçiğine de Pol. I enzimi yardımı ile ikinci
bir cDNA sentezlenerek çift iplikcikli DNA molekülü haline çevrilir. İşlemler, Southern blot tekniğindeki gibi yürütülür. Bazı durumlarda, geni,
DNA'dan değil de, bunun bir komplementeri olan ve hücre içinde sentezlenen mRNA'dan
yararlanılabilir. Bu durumda mRNA'ya komplementeri olan çift iplikcikli DNA sentezlenir. Yukarıda bahsedilen ve
genin yerinin belirlenmesi ve izolasyonuna yönelik çalışmalar oldukça uzun, zaman
alıcı ve bazen de başarısız olabilmektedir. Bu nedenle, pratikte daha etkin olan
basit uygulamalar kullanılmaktadır. Şöyle ki, bir RE ile kesilerek çeşitli boylarda
DNA segmentleri elde edildikten sonra klonlama işlemine geçirilir ve gen taşıyan
bakteri kolonileri seleksiyonla seçilerek
saf olarak üretilir ve genin ekspresyonu araştırılır. Aşağıda bu teknik izah
edilmektedir.
DNA'larında istenen
geni taşıyan bakteriler üretildikten ve DNA'ları çıkarıldıktan sonra
saflaştırılır ve bir süspansiyon elde edilir. Bu DNA süspansiyonu bir (veya
gerekirse iki) restriksiyon endonukleaz ile
muamele edilerek DNA'lar değişik boylarda olmak üzere çok sayıda segmente bölünür.
Doğaldır ki bu kadar çok sayıda segment (genomik DNA fragmenti) arasında istenilen
(hedef) geni taşıyan sayısız sekans bulunacaktır. Elde edilen DNA fragmentleri, ayrı
ayrı uygun vektörle bağlandıktan sonra klonlanır. Agar üzerinde oluşan koloniler,
istenilen gen (hedef gen) yönünden teker teker incelenirler. Aracı moleküllerle
(vektör DNA'sı ile) birleşecek olan segmentler, vektörlerin (plasmid, faj, fajmid,
cosmid, vs.) bakteri içindeki üremesini engellemeyecek bir boyutta ve en önemlisi de
iyi eksprese olması gereklidir. Bu nedenle, vektörle birleşen her DNA segmentinde
istenen gen bulunmadığı gibi, gen içeren çok büyük veya küçük segmentler de
vektörlerle birleşseler bile, bakteriye girmeyebilir veya girse bile eksprese
olmayabilirler. Klonlamada
yararlanılan bazı restriksiyon endonukleazlar bakteri genomunda kesme yaptıktan sonra
oluşan segmentlerin uçları bir birinin komplementeri olup yapışkan bir özellik
taşırlar (yapışkan
uçlar, cohesive ends). Oluşan bu serbest uçlar tekrar birleşebilir ve sirküler
bir durum alabilirler (resirkularizasyon). Bu özelliğe, vektör DNA'sında da
rastlanır. Her RE'nin kesiş yeri farklı olduğu gibi oluşturduğu yapışkan uçların
baz sıraları ve sayıları da değişiktir. Gerek bakteriye ait DNA
segmentlerinin ve gerekse vektör DNA'sının kendi aralarında tekrar birleşmesi,
rekombinant DNA molekülü elde etmede güçlükler yaratmakta ve gen segmentinin
vektörle birleşmesini önlemektedir. Bu olumsuz duruma mani olmak için bazı
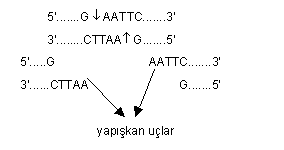
metotlardan yararlanılır. Eğer genomik DNA
(bakteri kromozomu), EcoRI enzimi ile kesilmişse, kesik yerlerin uçlarında birbirinin
komplementeri olan ve kolayca birleşen iki yapışkan uç meydana gelir. Bu durum
aşağıda gösterilmiştir (EcoRI için). EcoRI enzimi DNA da 6
bazlık bölgeden ve G/A arasından karşılıklı (asimetrik) olarak keser. Eğer segment
6 bazdan çok uzunsa, tam bir kopma gerçekleşemez. Buna benzer durum aynı enzimle
kesilen vektör DNA'sında da oluşur. Resirkülarizasyonu
önlemek için bazı yöntemlerden yararlanılır. Bunlardan bazıları çok kısa olarak
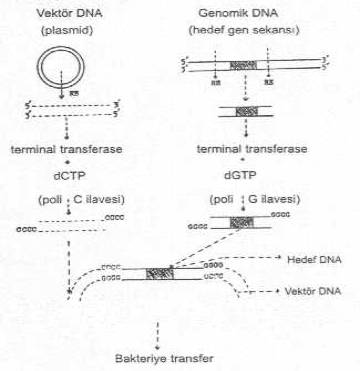
belirtilmiştir. 1) Kopolimer (homopolimer) ile kullanılması: EcoRI, (PstI, Hind III, vs. gibi) ile kesilerek oluşturulan yapışkan uçlar, enzimatik (Nukleaz S1) yöntemlerle kesilerek çıkarılır ve küt uçlar oluşturulur. Bu uçlara 3'-uçlarına, kopolimer segmentler (poli G veya poli C gibi) ilave edilerek DNA segmentlerinin her iki ucunda birbirleriyle birleşmeyen poli G(GGGG....G) veya poli C(CCCC...C) uçları meydana gelir. Aynı segmentin her iki ucunda poli C veya sadece G olursa bu segmentler resirkülarize olamaz. Çünkü, poli C'lar birbirinin komplementeri değildir. Kopolimer segmentleri ilave etmede terminal nukleotid transferaz (terminal transferaz) enziminden yararlanılır.
Burada önemli olan
nokta, genomik hedef
gen sekanslarının 3'- uçlarına poli G ilave edilmişse, vektör DNA'ya poli C ilave
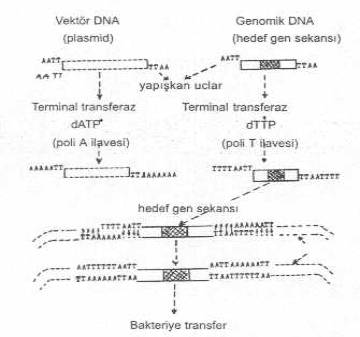
edilir (her iki ucuna). Bazı durumlarda,
yapışkan uçlar giderilmeden de kopolimer segmentler ilave edilebilir ve
resirkularizasyon önlenebilir. Yapışkan uçların kapatılması, bu uçların kalıp
olarak kullanılması ile gerçekleştirilir.
Her iki tarzda, eğer
genomik DNA segmentleri için poli G'ler (veya poli C'lar) kullanılmışsa, aynı enzimle
kesilen vektör DNA uçlarında bu sefer C (veya poli G ler) kullanılarak, vektör
DNA'sı ile genomik DNA segmentleri arasında birleşme sağlanır. Bu uçlar
birbirlerinin komplementeridirler. 2) Alkaline fosfotase kullanılması: Yapışkan
uçları gidermede dana intestinal alkaline fosfotase enzimi, bakteriyel alkaline
fosfotase enzimine, tercih edilmektedir. Bu enzim DNA segmentinin iki ucundaki fosfat
moleküllerini (5'-P) çıkararak resirkularizasyonu önler. Bu enzimle sadece vektör DNA
muamele edilir, genomik DNA segmentlerine uygulanmaz. Çünkü, bunlarda bulunan 5'-P ucu
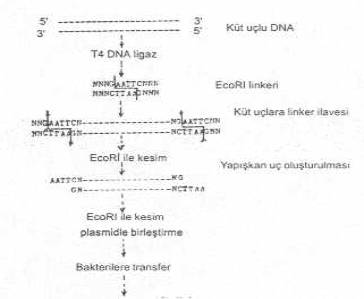
birleşme için yeterlidir. 3) Spesifik linkerlerin kullanılması:
Çalışmanın amacına uygun olarak, Hae III, Bal I, HpI, vs. gibi enzimlerin biri ile
kesilerek oluşturulan küt uçlara (veya yapışkan uçlar çıkarılarak meydana gelen
küt uçlara) sentetik çift iplikcikli oligonukleotidlerden oluşan spesifik linkerler
(adaptör moleküller) ilave edilir. Ancak, bu moleküllerin yapışkan uç
oluşturacak enzimlerden biri için (Örn., EcoRI, PstI, Hind III, vs.) spesifik kesim
bölgelerine sahip olması gerekir. Bu nedenle de EcoR1 linkeri, PstI linkeri,
vs. gibi isimler ile anılırlar. Bu linkerler ilave edildikten sonra, kendine ait RE ile
kesilerek yapışkan uç meydana getirilir, gerekirse benzer işlem vektör DNA'da da
yapılabilir.
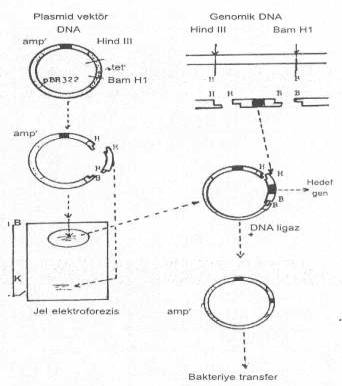
4) İki ayrı RE ile kesim: Yukarda açıklanan
yöntemlerden ayrı olarak, bir enzim yerine, yapışkan uç oluşturan iki ayrı enzim de
kullanılabilir. Şöyle ki, vektör DNA, Hind III ve Bam HI ile kesilince, vektör
DNA'sının bir ucunda Hind III ve diğer ucunda da Bam HI'e ait yapışkan uçlar meydana
gelir. Bu uçlar birbirinin komplementeri olmadığı için birleşemezler. Aynı işlem,
genomik DNA segmentleri için de uygulanır. Bunlar da kendi aralarında birleşemezler.
Bu aşamadan sonra, vektör DNA segmentleri jel elektroforezine tabi tutularak büyük
segmentler çıkarılır ve genomik DNA segmentleriyle birleştirilirler.
Eğer denemede, vektör
olarak pBR322 plasmidi kullanılmışsa tetr
geni hem Hind III ve hem de Sal I ile kesilince genden bir küçük segment koparılır.
Böylece gen inaktive olur. İşte, vektörün geride kalan büyük segmentinin
uçlarında farklı yapışkan uçlar olacağından birleşme de (resirkularizasyon)
olamaz. Elektroforezden sonra, bu büyük segmentler, çıkarılarak in vitro koşullarda
genomik DNA segmenti ile birleşmeye tabi tutulur. Çünkü, bu da iki enzimle kesilerek
hem Hind III ve hem de Sal I'e ait yapışkan uçlara sahiptir. 5) Küt uçların kullanılması: Olanaklar
yetersiz olduğu durumlarda küt uçlar, DNA ligaz enzimi ile birleştirilmeye
çalışılabilir. Ancak, çok zayıf bir birleşme olur ve bu işlem zaman alıcıdır.
Onun için küt uçlar pek kullanılamazlar. 6) Çok sayıda genomik
DNA segmenti ve vektör DNA kullanarak da resirkularizasyon riski azaltılabilir. 05.
Vektör DNA'nın Elde Edilmesi Yukarıda
açıklandığı tarzda hazırlanan genomik DNA segmentleri ile vektör DNA'sı
birleşecek duruma getirilir. Diğer bir ifade ile her iki DNA uçlarında karşılıklı
birleşmeye elverişli yapışkan uçlar sağlanır. Eğer genomik DNA'da Hind III
kullanılmışsa, vektör DNA'da da aynı RE, yani Hind III, kullanılmalıdır. RE'ler, büyük olan
genomik DNA üzerinde çok sayıda kesim yerlerine sahiptir. Bu nedenle, değişik
boylarda çok sayıda DNA segmentleri meydana gelebilir. Durum, vektör DNA'ları için de
benzeridir. Ancak, bazı RE'lerin vektör DNA üzerinde hiçbir kesim yerine sahip
olmamasına karşın, diğerlerinin 1, 2, 3.... çok sayıda kesim yeri olabilir ve
vektör DNA'da değişik boyda segmentler oluşabilir. Rekombinant DNA molekülü elde
etmede, vektör DNA'da sadece bir kesim yerine sahip olan RE'ler (Örn., Hind III. Sal I,
Pst I, vs.) tercih edilir. Bu enzimler vektör DNA'yı kestiklerinde hem yapışkan uçlar
meydana getirirler ve hem de sirküler vektör DNA'sını sadece açarlar. Herhangi bir
parça koparıp çıkarmazlar. Vektörlerde bulunan
antibiyotik rezistenslik (ampr, tetr, vs.) genlerinden biri RE ile kesilerek
ayrılır ve bunun içine yabancı gen aktarılarak gen inaktive edilir. Genomik DNA'da bir RE
ile kesimde, çok sayıda kesim yeri olduğundan, değişik boylarda ve fazla miktarda DNA
segmentleri meydana gelecektir. Prokaryotik veya bir ökaryotik tek bir hücre genomunda
istenilen gen veya klonlanması arzu edilen hedef gen, genellikle, bir tanedir. Bu da RE
ile kesimde meydana gelen DNA segmentlerinden birinde bulunur. Ancak, klonlamada tek bir
hücre genomu değil de milyarlarca hücre DNA'sı kullanıldığına göre, milyarlarca
hedef gen taşıyan genomik DNA segmenti ve bunun da yüzlerce (hatta binlerce) katı
sayıda istenilen geni taşımayan (ancak, diğer genleri taşıyan) fragmentler
oluşacaktır. Bu nedenle, genomik DNA (gen DNA'sı) ile vektörün birleşmesini
garantilemek için, birleşme işlemi aşamasında çok sayıda vektör kullanmak
gerekecektir. Eğer vektör olarak plasmid kullanılacaksa, bunun da uygun metotlarla
sayısının çok artırılmasına çalışılmalıdır. Birleşme aşamasında
kullanılacak vektörün amaca uygun olarak seçilmesi ve iyi yöntemlerin kullanılması
uygun sayıda hibrid DNA'sı elde etmek için gereklidir. Vektörlerde bazı spesifik
markerlerin (ampr, tetr, kanr,
lac+, vs.) bulunması, istenilen
geni taşıyan kolonileri bulmada büyük yardımcı olurlar. Klonlamada doğal plasmidler
yerine suni plasmidlerden daha çok yararlanılır. 06. Gen DNA'sının
Vektör DNA'sı
ile Birleştirilmesi Yukarıda belirtildiği
tarzda ve saf olarak hazırlanan genomik DNA segmentleri ile vektör DNA (eğer plasmid
ise) 37°C - 40°C'de birlikte 3-5 dakika inkubasyona bırakılır. Böylece,
karşılıklı yapışkan uçların birleşmesi sağlanır. Yapışkan uçları birbirine
bağlamada, ortama, DNA ligaz enzimi de
ilave edilir ve birleşme sağlamlaştırılır. DNA ligaz enzimi bu işlevini, DNA'nın
bir ucundaki 5'-P ile diğer DNA'nın 3'OH ucu arasında fosfodiester bağları kurarak
gerçekleştirir. Bu birleşmenin
gerçekleşmesi için alternatif yöntemler de bulunabilir. Gerekirse onlar da
denenebilir. Araştırıcılar,
kendi deneyimlerine, bilgilerine ve olanaklarına göre en uygun ve etkili olanını
seçebilirler. Bu işlem sonunda
birleşen moleküller (rekombinant
plasmid) oluşabileceği gibi resirkularizasyon nedeniyle birleşmeyen genomik DNA
segmentleri ve plasmid DNA'sı da meydana gelebilecektir. Ayrıca, plasmidle sadece genomik DNA segmenti değil, ortamda
çok sayıda bulunan diğer genleri taşıyan veya taşımayan ve uygun uzunluktaki
segmentler de birleşebilirler. 07. Rekombinant
Plasmid DNA'sının Alıcı
Hücreye Aktarılması Vektör olarak
plasmidlerin (pBR322, pUC, vs.) kullanıldığı durumlarda alıcı hücre olarak ta bu
plasmidlerin ait olduğu uygun konakcı E. coli (veya eğer plasmid bir basile ait ise, alıcı
hücre de, uygun bir basil olmalıdır. Örn., pUB110 plasmidi B. subtilis 'e aittir), seçilerek kullanılır. Vektör ve genomik DNA
segmentleri birleşmesinden oluşan konjugat, yeteri miktarda konakcı E. coli ile birlikte bulundurulduktan sonra, içinde
uygun bir sıvı besi yeri ve Ca+2
iyonları bulunan erlenmayere transfer edilirler.
E. coli 60-90 dakika kadar
37°C'de üretilir. Ortama katılan CaCI2
E. coli 'nin yüzeyini, sirküler
plasmid DNA'sı için geçirgen hale getirir ve rekombinant plasmid kolayca bakteriye
transfekte olur
(transfeksiyon). Bu inkubasyon
sırasında başlıca 4 durum meydana gelebilir. 1) Hiçbir plasmid
içermeyen E. coli 'ler, E. coli ile
rekombinant plasmid DNA'sı (pBR322) uygun ısıda bırakılırsa yaklaşık 60 dakikalık
bir inkubasyondan sonra erlenmayerde milyarlarca mikroorganizma meydana gelecektir. Ancak,
yabancı genlerin E.coli 'ye girme
oranı 10-8 - 10-9 arasındadır. Bu bakımdan çok fazla
mikroorganizma kullanılmalı ve çok iyi bir seleksiyon yapılmalıdır. Denemede kullanılan
alıcı suş E. coli 'de
rezistenslik faktörleri taşıyan hiçbir plasmid bulunmamaktadır. Bu nedenle de amp ve
tet’e duyarlıdır ve bu nedenle de her iki antibiyotiği ayrı ayrı veya birlikte
içeren besi yerinde üremezler. 08. İstenilen Geni
Taşıyan E.
coli 'lerin Seçimi (Seleksiyon) İstenilen geni
taşıyan plasmidli E. coli kolonilerini diğerlerinden ayırmak, gen aktarma
tekniğinin en önemli bir aşamasını oluşturur. Bunu sağlamak için, 1) Koloni seleksiyonu: Sıvı ortamda üretilen Saf E.
coli kültüründen içinde amp ve tet
içeren yarı katı besi yerlerine ayrı ayrı ekilir ve üretilirler. a) Eğer E. coli içine hiç plasmid girmemişse, bu E. coli 'ler her iki ortamda da üreyemezler. Çünkü,
dirençlilik genleri almadıklarından ve kendisinde de bulunmadığı için bir koloni
oluşturamazlar (madde 1). Bu durum karşısında,
ampisilinli ortamda üreyip te, tetrasiklinli ortamda üreyemeyen kolonilerden biri
seçilerek saf olarak üretilir ve deneme bir defa tekrar edilir (ekimler replica plating tarzında yapılır ve koloni
seçimi ampisilinli ortamdan yapılır). Durum aynı ise, seçilen koloni saf olarak
üretilir ve E.coli 'ler içinde
istenilen genin var veya yok olduğu araştırılır. Vektör DNA olarak pUC8/9
plasmidinden yararlanılmış ve bu plasmidin laktoz geni (beta galactosidase) RE ile kesilerek buraya
yabancı gen yerleştirilmişse, bu genin aktivitesi ortadan kalkar. Eğer, böyle bir
konjugat (kimerik plasmid) taşıyan E. coli,
ampisilin ve Xgal (5-bromo -4chloro -3-indolyl -beta- D-
galactopyronoside) içeren ortama aktarılırsa, E.coli ler ürer ancak,
enzim sentezlenemediği için Xgal'ı
ayrıştıramaz ve kolonilerin etrafı renksiz olarak görülür. Bu tür koloniler (lac,
ampr) seçilir ve saf olarak üretilir. Eğer
beta galactosidase geni sağlamsa, inaktive olmamışsa, sentezlenen enzim, Xgal'ı ayrıştırarak koloni etrafında mavi
renk meydana getirir (lac+, ampr dirençli
koloniler). Ancak, her iki tür
plasmidle yapılan böyle çalışmalarda da, istenilen gen ile diğer yabancı gen veya
DNA sekanslarını taşıyan plasmidli E. coli 'leri birbirinden ayırmak oldukça
güçtür. Kolonilerin teker teker ve saf olarak üretilip genin ekspresyonu kontrol
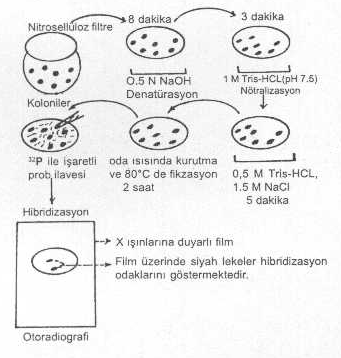
edilmelidir ki bu da oldukça zahmetli ve zaman alıcı bir işlemdir. Bunun yerine, 2) Koloni hibridizasyonu: Tetrasiklinli ortamda
üremeyip te ampisilinli besi yerinde üreyen kolonilerden saf kültür yapıldıktan
sonra, kültürden bir agarın yüzeyinde düzgün ve uygun aralıklarla nokta tarzında
ekimleri yapılır. Uygun bir ısı ve süre inkubasyona bırakıldıktan sonra,
kolonilerin iyi gelişmesi sağlanır. Sonra kolonilerin üzerine bir filtre kağıdı
değdirilir ve koloniler simetrik olarak kağıda geçirilir. Kağıt 0.5 N NaOH ile
muamele edilerek, bakterilerin denatürasyonu (iki
iplikcikli DNA'nın tek iplikcikli hale dönüştürülmesi) sağlanır. Tek iplikçikler
kağıda fikse edildikten sonra, üzerine radyoaktif (32P)
tek iplikçik cDNA veya RNA prob ilave edilir ve
bir süre bekletildikten sonra (hibridizasyon için) prob ile komplementer olan bakteri
DNA tek iplikçiği birleşir ve çift iplikcikli radyoaktif DNA segmenti oluşur (hibridizasyon).
Bundan sonra, üzerine X-ışınlarına duyarlı film kapatarak,
radyoaktivitenin filme etkilemesi sağlanır (Otoradyografi). Film
üzerindeki radyoaktif bölgeler siyah
lekeler halinde görülür. Bu bölgelerde istenilen gen DNA'sı olduğundan, agar
üzerinde yeri belirlenir ve koloniler alınarak istenilen gen yönünden incelenirler.
3) Dot blot hibridizasyonu: Bakterilerde plasmidin
aranmasında, işaretli problar kullanılarak dot blot hibridizasyon yönteminden
yararlanılabilir. a) Eğer, gen ürünü
protein, bakteri içinde kalıyorsa ve dışarı çıkamıyorsa, bu zaman gen ürününe
karşı tavşanlardan elde edilen antikorlar (monoklonal antikor daha duyarlıdır) 32P ile işaretlenir. Agar üzerinde üremiş ve
kloroform buharına tutularak lize edilmiş mikroorganizmalar buradan nitroselüloz
kağıtlarına aktarılır ve fikse edilir. Mikroorganizma içinde bulunan gen ürünü
proteinler (antijenler) de kağıt üzerinde fikse edilirler. İşaretlenmiş antikorlar,
bu proteinler üzerine yayılarak birleşmesi (antijen-antikor
reaksiyonu) sağlanır. Otoradyografi ile,
birleşen yerler, siyah lekeler halinde ortaya çıkarlar. b) Gen ürünü
proteinler hücrelerden dışarı çıkıyorsa, agar jel diffüzyon
yönteminden yararlanılabilir. Agara, gen ürününe karşı hazırlanmış
antikorlar katıldıktan sonra, açılan deliklere mikroorganizma ekstraktları konur.
Uygun bir inkubasyon süresi sonunda antijen içeren deliklerin etrafında oluşan
presipitasyon çizgilerine göre değerlendirme yapılır. c) Bakteri
ekstraktları ile, ELISA ve RIA gibi teknikler de kullanılarak genin
eksprese olduğu ve istenen gen ürününü sentezinin sağlandığı ortaya konabilir. 09.
Gen Ürününün Kontrolü Bakteri içinde, veya
aynı zamanda dışa salgılandığı durumlarda filtratlardan, gen ürünü saptandığı
hallerde aktivite, saflık, zararsızlık, yan etkileri vs., etkinliklerinin dikkatlice
incelenmesi gerekmektedir. Bakteri içinde veya filtratlarda bulunan gen ürünleri,
bakterilere ait endo- ve ekzo proteinlerle, toksin veya toksik substanslarla, enzimlerle,
metabolitlerle, vs. yabancı ve zararlı maddelerle kontamine olabilirler. Bu nedenle gen
ürününün bunlardan ayrılması ve saf olarak elde edilmesi (pürifikasyon) gereklidir. Bunun ilk
aşamasını klonlamada kullanılan mikroorganizmaların iyi seçilmesi oluşturur.
Ayrıca, bakteri içinde bulunan endoenzimler ve dışa salgılanan ekzoenzimler
(hidrolitik enzimler) sentezlenen gen ürünü proteinini hidrolize ederek ayrıştırabilir ve
etkinliğini bozabilirler. Bazen de gen ürünü, bakteri için toksik olabilir. Elde edilen ürünlerin, kobay, fare veya tavşanlarda toksisite testleri, yan etkileri ve etkinliği de araştırılır.Ayrıca, antijenik yeteneği de çeşitli immunolojik yöntemlerle belirlenir ve gerekli diğer kontrolleri de yapılır. Sonra çeşitli metotlarla saflaştırılır ve dozu ayarlanır. |
||||||||||||